Cydectin TriclaMox
ATC-Code
Tierarten
Rind.
Diagnosen
Zur Behandlung von Mischinfektionen mit Nematoden und Leberegeln sowie bestimmten ArthropodenInfestationen, die durch folgende Moxidectin- und Triclabendazol-empfindliche Stämme verursacht werden:
|
Parasit |
Adulte Stadien |
L4 |
Inhibierte Stadien |
|
NEMATODEN |
|||
|
Nematoden des Gastro-Intestinal-Traktes: |
|||
|
Haemonchus placei |
● |
● |
|
|
Ostertagia ostertagi |
● |
● |
● |
|
Trichostrongylus axei |
● |
● |
|
|
Nematodirus helvetianus |
● |
● |
|
|
Cooperia oncophora |
● |
● |
|
|
Cooperia punctata |
● |
||
|
Oesophagostomum radiatum |
● |
||
|
Bunostomum phlebotomum |
● |
||
|
Nematoden des Respirationstraktes: |
|||
|
Dictyocaulus viviparus |
● |
||
|
TREMATODEN |
|||
|
Leberegel: |
6 – 8 Wochen alte, unreife Stadien |
||
|
Fasciola hepatica |
● |
● |
|
|
EKTOPARASITEN |
|||
|
Linognathus vituli |
● |
||
|
Bovicola bovis |
● |
||
|
Solenopotes capillatus |
● |
Das Tierarzneimittel hat einen persistierenden Effekt zur Vermeidung einer erneuten Infektion durch Ostertagia ostertagi und Dictyocaulus viviparus für 5 Wochen nach einer Einzeldosis.
Wartezeit
Essbare Gewebe: 143 Tage.
Milch: Bei Rindern, deren Milch für den menschlichen Verzehr vorgesehen ist, in keinem Alter anwenden.
Aufgrund der hohen Wahrscheinlichkeit einer Kreuz-Kontamination von nicht behandelten Tieren mit diesem Tierarzneimittel durch Fellpflege (Lecken) sollten behandelte Tiere während der Wartezeit getrennt von nicht behandelten Tieren untergebracht werden. Die Nichteinhaltung dieser Empfehlung kann zu Überschreitungen von Rückstandshöchstmengen bei nicht behandelten Tieren führen.
Dosierung und Art der Anwendung
Nur zur äußerlichen Anwendung.
0,5 mg Moxidectin/kg Körpergewicht und 20 mg Triclabendazol/kg Körpergewicht (entspr. 1 ml der Lösung für 10 kg) zur einmaligen äußerlichen Anwendung.
Zum direkten Auftragen auf Haut und Haare entlang der Mittellinie des Tierrückens vom Widerrist zum Schwanzansatz.
Nur auf sauberer, gesunder Haut anwenden.
Das Körpergewicht sollte so genau wie möglich bestimmt werden, um eine korrekte Dosierung zu gewährleisten. Die Genauigkeit der Dosiereinrichtung sollte überprüft werden.
Wenn Tiere eher gemeinsam als individuell behandelt werden sollen, sollten sie entsprechend ihres Körpergewichtes und der Dosierung gruppiert werden, um Unter- oder Überdosierungen zu vermeiden.
Vor der Anwendung schütteln.
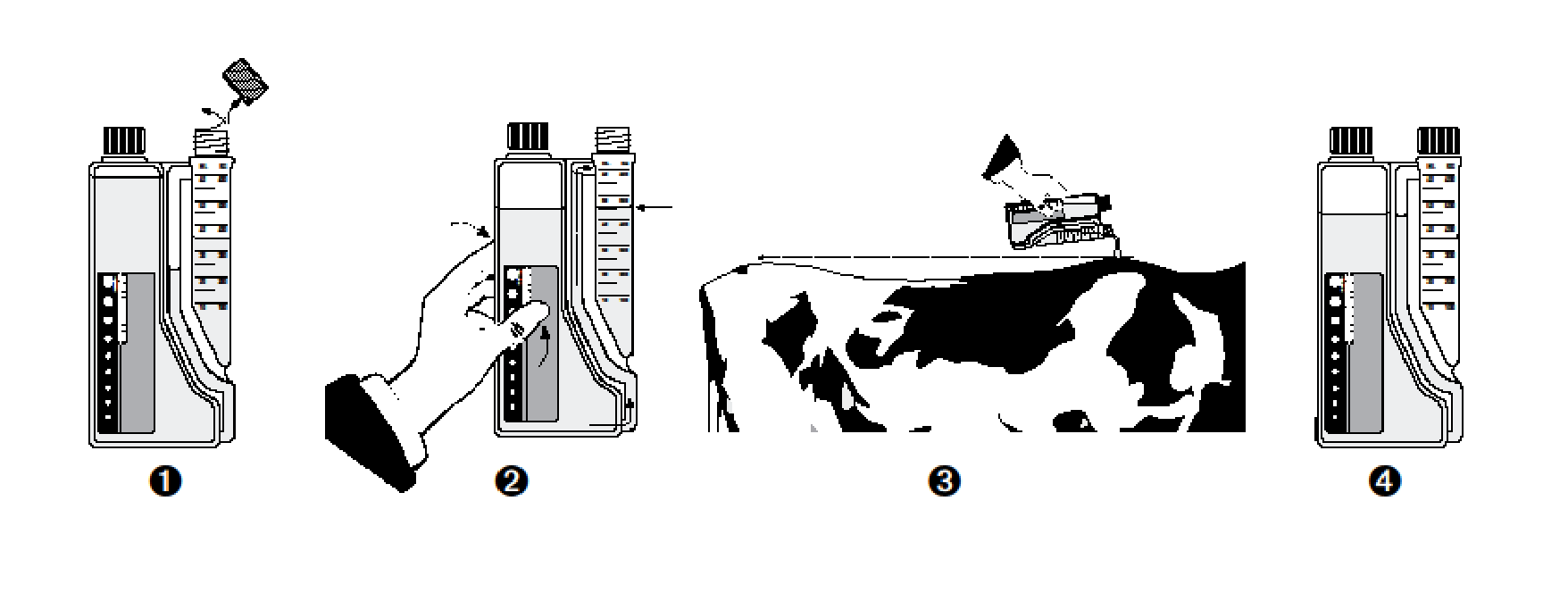
Gebrauchsanweisung für das Squeeze-Pour System (nur 500 ml und 1 l Flaschen): Schritt 1: Entfernen Sie die Schraubkappe nur von der Dispensierkammer. Entfernen Sie die Foliendichtung.
Schritt 2: Drücken Sie nun die Flasche behutsam, um die Messkammer mit der erforderlichen Flüssigkeitsmenge zu befüllen.
Schritt 3: Gießen Sie das abgemessene Volumen der Flüssigkeit direkt von der Kammer auf das Tier.
Wiederholen Sie die Schritte 2 und 3 für nachfolgende Tiere.
Schritt 4: Nach der Anwendung Dispensierkammer wieder mit der Schraubkappe verschließen.
Gebrauchsanweisung für den Pour-on Applikator (2,5 l und 5 l Rucksack):
Verbinden Sie den Pour-on Applikator mit dem Rucksack wie folgt:
Schließen Sie das offene Ende des Ansaugschlauches an die Kappe mit dem Schlauchschaft an. Ersetzen Sie die Versandkappe durch die Kappe mit dem Ansaugschlauch. Ziehen Sie die Kappe mit dem Ansaugschlauch fest.
Befüllen Sie den Pour-on Applikator behutsam, überprüfen Sie dabei, ob Lecks vorhanden sind.
Folgen Sie den Herstelleranweisungen für die korrekte Anwendung und die Pflege der Apparatur.
Nebenwirkungen
Rind:
|
Sehr selten (< 1 Tier/10 000 behandelte Tiere, einschließlich Einzelfallberichte): |
Reizung an der Applikationsstelle Störungen des Verdauungstrakts (z.B. Durchfall) Überempfindlichkeitsreaktion Neurologische Störungen (z.B. Ataxie) |
Die Meldung von Nebenwirkungen ist wichtig. Sie ermöglicht die kontinuierliche Überwachung der Verträglichkeit eines Tierarzneimittels. Die Meldungen sind vorzugsweise durch einen Tierarzt über das nationale Meldesystem an das Bundesamt für Verbraucherschutz und Lebensmittelsicherheit (BVL) oder an den Zulassungsinhaber zu senden. Die entsprechenden Kontaktdaten finden Sie in der Packungsbeilage. Meldebögen und Kontaktdaten des BVL sind auf der Internetseite https://www.vetuaw.de/ zu finden oder können per E-Mail (uaw@bvl.bund.de) angefordert werden. Für Tierärzte besteht die Möglichkeit der elektronischen Meldung auf der oben genannten Internetseite.
Literaturhinweis

| STATUS | Im Handel verfügbar |
|---|
 VERIFIZIERTE DATEN
VERIFIZIERTE DATEN







